近日,湖南省转化医学与创新药物工程技术研究中心主任、湘雅二医院药学部向大雄教授团队在纳米药物治疗肿瘤领域取得最新研究进展,在生物材料国际期刊《Bioactive Materials》(2021 IF=16.874,JCR1区)上发表题为“Bacterial outer membrane vesicles-based therapeutic platform eradicatestriple-negative breast tumor by combinational photodynamic/chemo-/immunotherapy”的研究。论文第一作者及通讯作者单位均为中南大学湘雅二医院,向大雄教授为通讯作者,团队2019级博士研究生李泳江、吴军勇博士为共同第一作者。

细菌外膜囊泡(OMVs)是由革兰氏阴性菌分泌的天然球形囊泡,粒径在30-250 nm,含有多种病原相关分子模式(PAMPs),如脂多糖、肽聚糖、脂类等,是一种强烈的免疫刺激佐剂,是驱动机体固有免疫的有效因素。多项研究表明将OMVs用于疫苗可以诱导持久的体液和细胞免疫反应。然而,课题组研究发现在原位乳腺癌小鼠中静脉注射OMVs虽然可以一定程度激活免疫达到抗肿瘤目的,但是随着OMVs浓度增加会造成较严重的安全性问题,且单独应用OMVs抗肿瘤疗效有限。
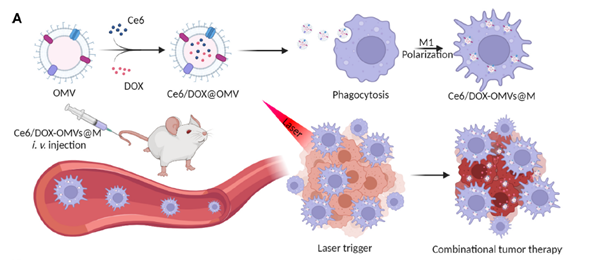
基于以上问题,课题组应用OMVs包载了化疗药物阿霉素(DOX)和常用的光敏剂Ce6,同时利用单核巨噬细胞肿瘤靶向和病原体吞噬原理将其作为“便车”搭载OMVs,构建了一种载OMVs巨噬细胞递药系统Ce6/DOX-OMVs@M用于靶向治疗乳腺癌。研究结果表明Ce6/DOX-OMVs@M可精确靶向至小鼠原位乳腺癌,经660 nm波长光照后巨噬细胞发生破裂释放载药OMVs,可极大增加OMVs的体内安全性。其中OMVs可重编程肿瘤巨噬细胞为M1型(抗肿瘤作用),同时引起肿瘤细胞焦亡释放炎症炎子,将“冷肿瘤”转变为“热肿瘤”,进一步增强免疫效应。与此同时,Ce6经光照后产生活性氧ROS,化疗药物DOX可进一步杀伤肿瘤细胞,达到“一石三鸟(光动力-化疗-免疫治疗)”目的,只需两次给药即可有效杀灭肿瘤且避免肿瘤细胞肺转移。本研究是在细菌及其分泌外膜囊泡用于肿瘤免疫治疗上的重要尝试和新的突破,构建的巨噬细胞给药系统可有效增加OMVs的安全性和肿瘤靶向性,为开发OMVs作为疫苗平台提供了新的思路。
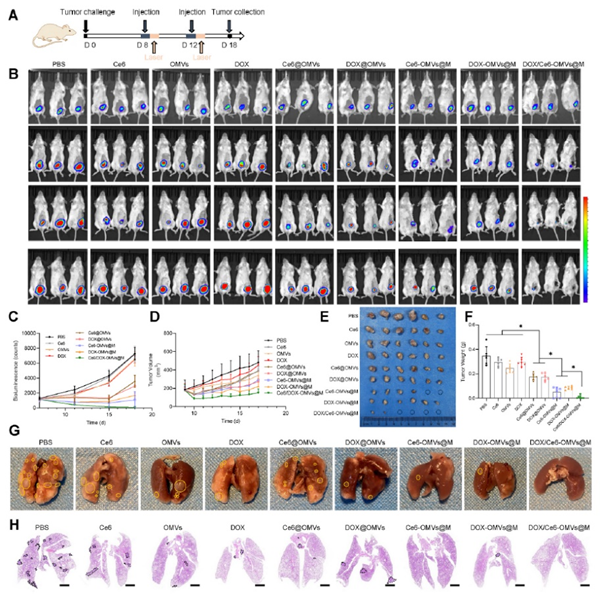
恶性肿瘤是严重危害人类健康的重大疾病,近年来发病率和死亡率逐年上升,而临床常规的治疗方式特异性差,毒副作用较大,使用常受到限制。精心设计的药物递送系统可以实现肿瘤的精准靶向,用以调控肿瘤的微环境或杀灭肿瘤细胞,达到减毒增效目的。然而常规的有机或无机纳米载体属于外源性材料,常引起机体的免疫响应,易被吞噬而失去效果。鉴于此,向大雄教授团队近年来着眼于仿生纳米递药系统研究,设计了一系列以囊泡、细胞膜等内源性材料为基础的纳米载体,实现了肿瘤的精准治疗,在《Journalofcontrolledrelease》(IF:11.467,3篇)、《Advancedhealthcarematerials》(IF:11.092,1篇)、《ActaBiomaterialia》(IF:10.633,1篇)、《JournalofNanobiotechnology》(IF:10.435,2篇)等国际期刊发表了多篇论文,其中2篇入选ESI高被引论文。
原文链接:https://www.sciencedirect.com/science/article/pii/S2452199X22002596
 扫码下载时刻APP
扫码下载时刻APP



